Internet a elektronické databázy stále viac približujú pacientom informácie o liekoch. Pacienti sa tak postupne v prístupe k informáciám približujú k možnostiam, ktoré majú odborníci v zdravotníctve. Potenciál týchto informácií si často ani neuvedomujú.Tento článok vysvetľuje charakter štandardizovaných dokumentov, v ktorých sú uchovávané a podávané informácie o liekoch. V druhej časti sú uvedené dôležité informačné zdroje o liekoch na internete.
Právne regulované dokumenty informujúce o liekoch
Dokument, ktorý je primárne určený pre pacientov a obsahuje informácie, ktoré by mali byť postačujúce pre bezpečné používanie lieku sa označuje ako Príbalová informácia pre pacienta (PIL – Patient Information Leaflet). Každý liek expedovaný v lekárni podľa zákona o lieku musí obsahovať vo forme priloženého letáku Príbalovú informáciu v slovenčine. Podoba dokumentu je štandardizovaná. Keďže formát sa v minulosti menil, môže sa stať, že lieky uvedené na trh v minulosti používajú starší formát.
Súhrn charakteristických vlastností lieku (SPC – Summary of Product Characteristics) je dokument určený primárne pre odborných zdravotníckych pracovníkov. Má štandardizovanú štruktúru a obsiahnuté informácie sú vo väčšine prípadov postačujúce pre rozhodnutie lekára o terapeutickom použití lieku. SPC má zároveň právne záväzný charakter, lieky musia byť predpisované v súlade s údajmi uvedenými v SPC. To znamená, že lekár môže určitý liek pacientovi predpísať iba pre indikáciu uvedenú v SPC, musí rešpektovať kontraindikácie a prípadné ďalšie obmedzenia. Výrobca lieku má povinnosť uviesť všetky známe nežiadúce účinky. Na rozdiel od PIL, ktorý má byť písaný tak, aby bol zrozumiteľný širokej verejnosti, SPC obsahuje viac odborných medicínskych výrazov, ako aj viac informácii o klinických štúdiách, takže nemusí byť pacientom dostatočne zrozumiteľný.
Popri informáciách v SPC a PIL, zákon stanovuje, ktoré informácie majú byť uvedené na obale lieku – sú to napríklad názov účinnej látky, držiteľa rozhodnutia o registrácii, doba exspirácie, alebo číslo šarže (dôležité pri stiahnutí z trhu, ak bola zistená závada vo výrobnom procese). Podobne informácia o názve lieku, účinnej látke, dobe exspirácie a šarži obsahuje aj každý blister.
Pri čítaní vyššie uvedených dokumentov je potrebné si uvedomiť spôsob, akým sú vytvorené (na základe právnej požiadavky a štandardizovaného obsahu) určuje ich charakter, niekedy aj v zmysle, ktorý môže byť problematický. Na základe všeobecne uznávaného vedeckého konceptu v medicíne tzv. Evidence Based Medicine (EBV) je možné o akomkoľvek lieku tvrdiť iba to, čo je jednoznačne vedecky dokázané v klinických štúdiách. Na druhej strane niekedy existujú dôvody, pre ktoré nie je možné klinickú štúdiu uskutočniť. Sú to najčastejšie etické dôvody – keď je problematické alebo neprípustné robiť klinický výskum napríklad na deťoch, alebo tehotných ženách, pokiaľ by skúšaný liek mohol viesť k trvalému poškodeniu plodu/dieťaťa. Napr. veľký počet liekov je kontraindikovaných pri tehotenstve a pri malých deťoch, pretože nebolo možné testovaním dokázať, že sú pre tieto skupiny bezpečné. Čo však neznamená, že sú pre nich nebezpečné.
Niekedy tiež vzbudzuje u pacientov veľké obavy množstvo nežiadúcich účinkov uvedených v PIL. Uvedenie všetkých nežiadúcich účinkov sa v súčasnosti vyžaduje zo zákona, pričom najzávažnejšie sa spravidla vyskytujú veľmi zriedkavo. Možno opodstatnene tvrdiť, že dnes sú na bezpečnosť liekov kladené prísnejšie požiadavky ako v minulosti. Prax pred niekoľkými desaťročiami bola skôr zriedkavé nežiadúce účinky do príbalovej informácie neuvádzať. Súčasný prístup odzrkadľuje väčší dôraz na bezpečnosť. Paradoxne sa niekomu môže zdať, že množstvo nežiadúcich účinkov „pribúda“ a lieky sú menej bezpečné.
Úzku súvislosť s poskytovaním informácii o liekoch má právna regulácia farmaceutického marketingu. Lieky, ktoré sú na predpis nemôžu byť v SR predmetom reklamy, ktorá je mierená k spotrebiteľom. Pripúšťa sa však ich reklama orientovaná na lekárov. Tá musí byť však zameraná na poskytovanie odborných informácií obsiahnutých v SPC. Následkom tejto „dvojsmernosti“ vychádzajúcej z legislatívy, sú v niektorých prípadoch formálne obmedzenie prístupu pacientov k verejne prístupným informáciám pre odborných zdravotníckych pracovníkov. Konkrétne sa jedná o niektoré internetové stránky, ktoré vyžadujú pre prístup k SPC potvrdenie, že používateľ je zdravotníckym odborníkom. Tieto stránky to však neoverujú a v praxi tieto ustanovenia o reklame prístup pacientov k informáciám neobmedzujú. Keďže legislatíva o regulácii farmaceutického marketingu vychádza z rovnakých princípov v celej EÚ, tieto formálne obmedzenia sú bežné aj na zahraničných internetových stránkach.
Pre úplnosť je vhodné dodať, že zďaleka nie všetky produkty s liečivými účinkami majú právny štatút liekov. Väčšina produktov určených na podpornú liečbu (vitamíny, minerály, probiotiká, špeciálne nutričné faktory a ich kombinácie) sú výživové doplnky a vzťahujú sa k nim vo všetkých smeroch menej prísne kritéria ako na lieky – neobsahujú PIL (iba predpísané informácie na etikete), aplikujú sa nižšie požiadavky na klinické skúšanie aj výrobu.
Na druhej strane každý liek má pridelený kód ŠÚKL (Štátny ústav pre kontrolu liečiv), ktorý ho jednoznačne identifikuje. Tento kód je často spoľahlivejší pri identifikácii lieku, ako jeho obchodný názov. Dôvodom je, že lieky sa často líšia iba počtom tabliet, obsahom účinnej látky alebo farmaceutickou formou.
Identifikátorom pre všetky farmaceutické produkty (lieky, výživové doplnky, kozmetické a ďalšie produkty), ktorý sa však bežne používa iba v elektronických databázach je ADC kód.
Zdroje na internete
ADC číselník (http://www.adcc.sk, predtým Nobelplus) je najkomplexnejšia a najnavštevovanejšia slovenská elektronická databáza farmaceutických produktov. Popri liekoch zahŕňa množstvo príbuzných tried produktov ako výživové doplnky, zdravotnícke potreby, veterinárne lieky, kozmetické výrobky. Vyhľadávanie je možné nielen podľa obchodného názvu, ale aj podľa ďalších kritérií ako názov účinnej látky, držiteľ rozhodnutia o registrácii. Ku každému lieku je k dispozícii PIL a SPC a množstvo ďalších údajov, vrátane informácie o cene a doplatku pacienta.
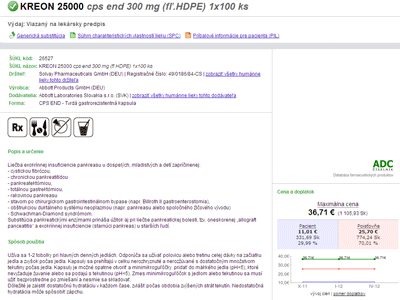
Vedľa odkazov na SPC a PIL nájdete tiež odkaz Generická substitúcia, ktorým sa zobrazia všetky registrované lieky s rovnakou účinnou látkou (generiká) s porovnaním ceny, samozrejme za predpokladu, že k danému lieku je k dispozícii generikum. Ikony pod základnými údajmi pomáhajú rýchlo sa orientovať v najdôležitejších údajoch o užívaní lieku, napr. či je liek viazaný na predpis, užívanie pri tehotenstve a laktácii. ADC číselník ponúka aj niektoré ďalšie služby – zverejňovaním odborných článkov funguje ako informačný portál v oblasti farmácie. Umožňuje aj overovanie interakcií (možnosť overiť si, ktoré lieky je možné spolu užívať bez rizika nežiadúcich účinkov vyplývajúcich z ich vzájomného podania), ale táto služba je spoplatnená. Ďalšie komerčné služby (eOrdering, NobelKOMPLET) sú určené pre subjekty na farmaceutickom trhu (lekárne, distribútorov).
Štátny ústav pre kontrolu liečiv (ŠÚKL, www.sukl.sk) má za úlohu vykonávať dohľad nad farmaceutickým trhom a na jeho stránkach môžete nájsť viacero užitočných informácii. Stránka ŠÚKL je primárnym zdrojom informácii o obmedzeniach v súvislosti s bezpečnosťou liekov. Na stránke v sekciách „Lieky a ZP – mimoriadne oznamy“ a „Aktuality“ sú zverejňované informácie o stiahnutiach (resp. uvoľneniach) z trhu. Dôvodom stiahnutia z trhu je spravidla problém s kvalitou lieku, ktorý sa zväčša vzťahuje ku konkrétnej šarži. Ak máte liek, ktorý bol stiahnutý, overte si jeho výrobnú šaržu ( uvádza sa na obale). Pokiaľ máte šaržu, ktorá nie je uvedená v ozname ŠÚKL ako stiahnutá, môžete liek ďalej užívať. Prostredníctvom mailing listu si môžete informácie o stiahnutiach nechať posielať emailom. Na stránkach ŠÚKL nájdete taktiež elektronickú databázu registrovaných liekov a zdravotníckych pomôcok. V porovnaní s databázou ADC obsahuje menej informácií (keďže ADC čerpá aj z ďalších zdrojov) a niekomu sa môže zdať databáza ŠÚKL zložitejšia, alebo menej používateľsky prístupná.
Ministerstvo zdravotníctva (http://www.health.gov.sk) prostredníctvom kategorizácie riadi cenotvorbu liekov. Ako je uvedené vyššie, informáciu o cene a doplatku k lieku je možné získať aj napríklad v ADC číselníku, kde je to spravidla aj jednoduchšie. Kategorizácia vychádza v tlačenej podobe vo vestníku MZ SR a v elektronickej podobe (xls súbor) je zverejňovaná na adrese http://www.health.gov.sk/?kategorizecia-a-uuc . Lieky sú v kategorizácii zoradené podľa terapeutických skupín (ATC systém) a obsahuje aj ďalšie kategórie číselných údajov (MCV, úhrada zdravotnej poisťovne, absolútny a percentuálny doplatok pacienta), čo pre laika môže pôsobiť neprehľadne.
Úrad verejného zdravotníctva (ÚVZ, http://www.uvzsr.sk) je zodpovedný za dohľad nad niektorými kategóriami farmaceutických produktov (výživové doplnky, kozmetické produkty). Jeho stránka však obsahuje k problematike farmaceutických produktov iba málo informácii a nie je k dispozícii žiadna elektronická databáza produktov.
ÚVZ má však širšiu pôsobnosť, ktorá zahŕňa niektoré epidemiologické sledovania, okrem iných antibiotickú rezistenciu. Jedným z výstupov týchto aktivít je aj zaujímavý projekt Slovak National Antimicrobial Resistance Surveilance System (SNARS, www.snars.sk), pri ktorom sú elektronické databázy nástrojom uľahčujúcim terapeutické rozhodnutia. Jednoduchšie povedané, na základe aktuálnych údajov o rezistencii je lekár schopný vybrať antibiotikum, pri ktorom je najnižšia pravdepodobnosť rezistencie. Optimálne je vždy urobiť mikrobiologické vyšetrenie citlivosti, ktoré ukáže skutočnú citlivosť u konkrétneho pacienta. Mikrobiologické vyšetrenie však trvá niekoľko dní a možnosť začať s liečbou skôr je veľká výhoda. Liečba vychádzajúca z prehľadu epidemiologickej situácie sa označuje ako empirická terapia.
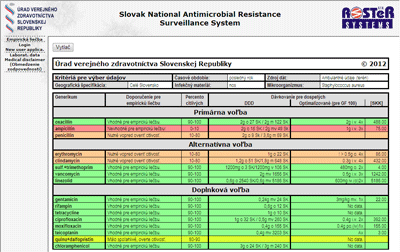
Stránka SNARS funguje iba pod prehliadačom Internet Explorer. Niektoré údaje sú voľne prístupné, pre ďalšie je potrebná registrácia. Je bezplatná a určená pre zdravotníckych pracovníkov. Bez registrácie (Empirická liečba) môžete zistiť odporúčané antibiotikum na základe údajov o rezistencii, pričom sa zohľadňuje pôvod materiálu (výter hrdla, spútum, moč, … ), geografická oblasť (kraj), ambulantný alebo nemocničný pôvod vzorky a predpokladaný pôvodca ochorenia. Po registrácii je možné vyhľadávanie údajov podľa presnejších kritérií (napr. rôzne časové rady, rôzne hodnoty MIC, mechanizmu rezistencie, diagnózy).
European Medicines Agency (EMA, http://www.ema.europa.eu) je najdôležitejšou Európskou inštitúciou v oblasti dohľadu nad farmaceutickým trhom. EMA udeľuje pri niektorých skupinách liekov povolenia na uvedenie na trh platné v celej EÚ (najmä originálne lieky, tie čo sú registrované centralizovanou procedúrou), zatiaľ čo u iných to zatiaľ zostáva kompetenciou miestnych štátnych liekových agentúr ako je v SR ŠÚKL (najmä generické lieky, registrované MRP, DCP a NP procedúrami). Stránka EMA môže byť lepším zdrojom informácii (ako vyššie uvedené slovenské stránky) najmä v nasledovných prípadoch: informácie o liekoch schválených centralizovanou procedúrou (napr. orphan , biotechnologicky vyrábané lieky), EMA (na rozdiel od ŠÚKL ako aj väčšiny národných liekových agentúr) má adekvátnu vedeckú kapacitu posudzovať často veľmi komplexné klinické a postmarketingové štúdie o účinku a bezpečnosti liekov a publikuje k týmto zisteniam správy. Internetová stránka EMA je vo všeobecnosti veľmi obsažná na informácie a používateľsky prívetivá. Ucelený prehľad Európskej liekovej legislatívy, vrátane odborných technických odporúčaní nájdete na adrese http://ec.europa.eu/health/documents/eudralex
Drugs.com (http://www.drugs.com) je jednou z množstva amerických stránok zameraných na informácie o liekoch. Zaujímavá je tým, že si prostredníctvom nej môžete (zdarma) overiť možnosť interakcií rôznych liekov (Interactions Checker). Pri možných liekových interakciách sa zobrazí podrobná informácia o mechanizme, akým k interakcii dochádza a aké sú možné následky. Zobrazia sa tiež možné interakcie s jedlom.
Zaujímavými prvkami sú pipeline databáza (zoznam podaných žiadostí o registráciu nových liekov), anglický medicínsky slovník, internetové fórum, alebo možnosť stiahnutia mobilných aplikácii. Je vhodné pripomenúť, že obchodné názvy, pod ktorými farmaceutické firmy predávajú svoje produkty sa často v jednotlivých krajinách líšia. To isté liečivo od tej istej farmaceutickej firmy má často v USA odlišný obchodný názov ako v Európe. Regulácia farmaceutickej reklamy je v USA o niečo voľnejšia ako v Európe.
Za istých okolností môže mať pacient prístup aj k liekom, ktoré zatiaľ nie sú schválené pre uvedenie na trh, ale sú v štádiu klinického skúšania. Je to možné, ak je pacient zaradený do klinickej štúdie. Pre zaradenie do štúdie sú vždy prísne medicínske kritéria. Globálnu databázu vrátane štúdii prebiehajúcich v SR vedie US National Institutes of Health, pričom databáza je prístupná na adrese http://clinicaltrials.gov. Stránka obsahuje množstvo údajov o skúšanom lieku, základné informácie protokolu štúdie a kontakty na sponzora štúdie. Na základe informácii o skúšanom lieku si môže lekár urobiť obraz o jeho potenciálnom prínose v prípade úspešnosti štúdie a schválenia uvedenia na trh.
Čo nenájdete na internete
Po prečítaní uvedených informácii, prípadne návšteve stránok, je zrejmé, že informácií, ktoré sa nedajú získať na internete, je už málo. Jednou z vecí, ktorá je ťažko overiteľná je dostupnosť produktu na trhu. Aj keď má liek platnú registráciu a nie je stiahnutý z trhu, môže byť nedostupný z iných dôvodov (problémy vo výrobe alebo logistike). V lekárni, kde využívajú elektronické objednávanie (dnes väčšina), si môžete na počkanie overiť, či je produkt k dispozícii. Zistíte tak, či je na sklade distribučnej firmy, a ak nie je na sklade, nie je ani možné odhadnúť, kedy by sa mohol znovu dostať do distribúcie. V takom prípade sa môžete obrátiť na medicínskeho reprezentanta farmaceutickej firmy, ktorý má na starosti konkrétny produkt. Medicínsky reprezentanti majú za úlohu poskytovať zúčastneným stranám (najmä odbornej, ale podľa požiadaviek aj širokej verejnosti) informácie o liekoch. Reprezentant môže mať lepší prehľad o situácii a pláne dodávok na trh a mal by vedieť zodpovedať všetky prípadné ďalšie odborné otázky o lieku, ktorý má v kompetencii. Kontakt na reprezentanta získate najľahšie prostredníctvom centrály farmaceutickej firmy, ktorá dodáva liek na trh. Spravidla majú farmaceutické firmy reprezentantov rozdelených podľa regiónov. V prípade, že má firma rozsiahly sortiment aj podľa portfólia.
